
îlots humains pour la Recherche
L’isolement d’îlots de Langerhans humains pour la recherche est réalisé à partir de pancréas ne répondant pas aux critères d’éligibilité pour la transplantation.
Les pancréas humains adressés par les coordinations locales du don d’organe, sont reçus dans notre laboratoire de recherche pour y être processés. Les îlots de Langerhans alors obtenus sont valorisés à travers les recherches internes ou dans le cadre de collaborations.
Ainsi, la plateforme PRIMS propose aux différentes équipes un accès aux collections biologiques d’échantillons humains tels que des îlots de Langerhans fraîchement isolés, des culots d’îlots, des fragments de tissus frais ou congelés ainsi que des coupes histologiques.
Les analyses en routine également proposées au laboratoire permettent d’évaluer la fonction sécrétrice des îlots, d’étudier leur viabilité, d’évaluer la pureté des préparations, de réaliser des analyses de biologie moléculaire ainsi que des marquages sur coupes histologiques.
Les préparations d’échantillons biologiques générées au laboratoire intègrent une collection d’échantillons humains déclarée au Centre de Ressources Biologiques (CRB) du CHU de Montpellier.
La plateforme PRIMS est accessible aux laboratoires académiques et industriels dans le cadre de collaborations ou de prestations de services après évaluation et validation du projet de recherche par les autorités compétentes. Des données associées peuvent être transmises avec le matériel biologique sur demande.



LTCD
Procédure d’isolement
Les pancréas sont obtenus à partir de donneurs PMO (prélèvements multi-organes) en état de mort cérébrale. Les pancréas sont prélevés et acheminés rapidement au centre isolateur de Montpellier dans le respect du délai d’ischémie froide (12h maximum). La procédure d’isolement débute dès réception du pancréas par l’équipe et dure entre 8h et 10h :
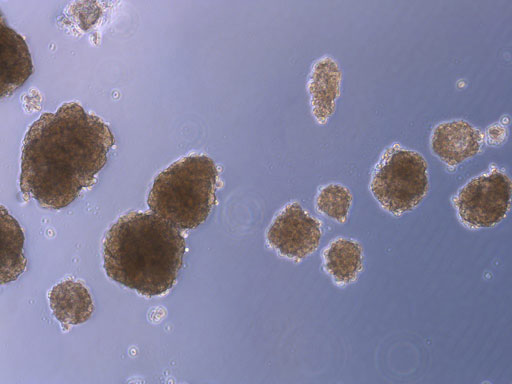
Le pancréas est correctement disséqué puis infusé par le canal pancréatique avec de la collagénase (enzyme de digestion) à 4°C. Le pancréas est ensuite placé dans une chambre de digestion (chambre de Ricordi) intégrée à un circuit de digestion fermé et chauffé à 37°C. Cette étape de digestion qui dure entre 20 et 30min permettra de digérer la partie exocrine du pancréas et de garder intact les îlots de Langerhans (partie endocrine). Au cours de cette étape cruciale, des échantillons sont régulièrement prélevés et observés au stéréomicroscope afin d’évaluer la qualité de la digestion et d’appréhender au mieux l’arrêt de cette étape, c’est-à-dire le moment où les îlots sont clairement dissociés du tissus exocrine. La prolongation de la digestion conduirait rapidement à abimer la structure des îlots de Langerhans et ainsi altérer leur fonction. L’activité de digestion par la collagénase est stoppée par dilution à 4°C.
La deuxième étape majeure de la procédure consiste à purifier les îlots de Langerhans du reste du tissu exocrine. Les îlots ayant une densité plus faible que la partie exocrine, ils sont donc séparés à l’aide d’un gradient de densité et par centrifugation (centrifugeuse COBE). Les îlots purs sont ensuite comptés, puis mis en culture dans un milieu adapté. Pour chaque procédure, la pureté, la viabilité ainsi que la fonction des îlots pancréatiques sont évaluées. De même, plusieurs tests microbiologiques sont réalisés au cours de la procédure.
Mise à disposition
Mise à disposition d’échantillons biologiques humains
-
Ilots de Langerhans fraîchement isolés.
-
Culots d’îlots de Langerhans congelés.
-
Fragments de tissus frais ou congelés.
-
Coupes histologiques (paraffine, cryostat).
Analyse de faisabilité, conseil, formation
Analyses en routine
-
Mesure de la fonction sécrétrice (hormones, cytokines) des îlots de Langerhans.
-
Etude de la viabilité (FDA/PI) des îlots de Langerhans.
-
Evaluation de la pureté des préparations.
-
Biologie moléculaire (Western-Blot, Extraction d’ARN).
-
Marquages sur coupes histologiques.



LTCD
Projets de Recherche
Le LTCD développe une recherche visant à améliorer l’isolement, la survie et la fonction sécrétrice des îlots pancréatiques humains afin de travailler à l’amélioration de l’efficacité des greffes.
Les projets de recherche plus fondamentale actuellement menés au laboratoire s’intéressent notamment à l’impact de la variabilité glycémique présente chez certains patients diabétiques sur la masse fonctionnelle des cellules β, au rôle de l’immuno-protéasome dans la régulation de la fonction des îlots humaine mais également à l’effet des cellules stromales pancréatiques immortalisées humaines sur la fonction et la survie des cellules β.
Bibliographie
- Targeting pancreatic islet PTP1B improves islet graft revascularization and transplant outcomes. Figueiredo H, Figueroa ALC, Garcia A, Fernandez-Ruiz R, Broca C, Wojtusciszyn A, Malpique R, Gasa R, Gomis R. Sci Transl Med. 2019 Jun 19;11(497). pii: eaar6294. doi: 10.1126/scitranslmed.aar6294. PubMed PMID:31217339.
- Indications for islet or pancreatic transplantation: Statement of the TREPID working group on behalf of the Société francophone du diabète (SFD), Société francaise d’endocrinologie (SFE), Société francophone de transplantation (SFT) and Société française de néphrologie - dialyse - transplantation (SFNDT). Wojtusciszyn A, Branchereau J, Esposito L, Badet L, Buron F, Chetboun M,Kessler L, Morelon E, Berney T, Pattou F, Benhamou PY, Vantyghem MC; TREPIDgroup. Diabetes Metab. 2019 Jun;45(3):224-237. doi: 10.1016/j.diabet.2018.07.006. Epub 2018 Sep 14. Review. PubMed PMID: 30223084.
- Proteasomal degradation of the histone acetyl transferase p300 contributes to beta-cell injury in a diabetes environment. Ruiz L, Gurlo T, Ravier MA, Wojtusciszyn A, Mathieu J, Brown MR, Broca C,Bertrand G, Butler PC, Matveyenko AV, Dalle S, Costes S. Cell Death Dis. 2018 May 22;9(6):600. doi:10.1038/s41419-018-0603-0. PubMed PMID: 29789539; PubMed Central PMCID:PMC5964068.
- Islet transplantation versus insulin therapy in patients with type 1 diabetes with severe hypoglycaemia or poorly controlled glycaemia after kidney transplantation (TRIMECO): a multicentre, randomised controlled trial. Lablanche S, Vantyghem MC, Kessler L, Wojtusciszyn A, Borot S, Thivolet C,Girerd S, Bosco D, Bosson JL, Colin C, Tetaz R, Logerot S, Kerr-Conte J, Renard E, Penfornis A, Morelon E, Buron F, Skaare K, Grguric G, Camillo-Brault C,Egelhofer H, Benomar K, Badet L, Berney T, Pattou F, Benhamou PY; TRIMECO trial investigators. Lancet Diabetes Endocrinol. 2018 Jul;6(7):527-537. doi: 10.1016/S2213-8587(18)30078-0. Epub 2018 May 15. PubMed PMID: 29776895.
- Pancreas preservation fluid microbial contamination is associated with poor islet isolation outcomes – a multi-centre cohort study. Meier RPH, Andrey DO, Sun P, Niclauss N, Bédat B, Demuylder-Mischler S, Borot S, Benhamou PY, Wojtusciszyn A, Buron F, Pernin N, Muller YD, Bosco D, van Delden C, Berney T. Transpl Int. 2018 Aug;31(8):917-929. doi: 10.1111/tri.13159. Epub 2018 Apr 16. PubMed PMID: 29603452.
- The Second Phase of Insulin Secretion in Nondiabetic Islet-Grafted Recipients Is Altered and Can Predict Graft Outcome. Villard O, Brun JF, Bories L, Molinari N, Benhamou PY, Berney T, Wojtusciszyn A. J Clin Endocrinol Metab. 2018 Apr 1;103(4):1310-1319. doi: 10.1210/jc.2017-01342. PubMed PMID: 29319810.
- Randomised, prospective, medico-economic nationwide French study of islet transplantation in patients with severely unstable type 1 diabetes: the STABILOT study protocol. Lablanche S, David-Tchouda S, Margier J, Schir E, Wojtusciszyn A, Borot S, Kessler L, Morelon E, Thivolet C, Pattou F, Vantyghem MC, Berney T, Benhamou PY. BMJ Open. 2017 Feb 20;7(2):e013434. doi: 10.1136/bmjopen-2016-013434. PubMed PMID: 28219959; PubMed Central PMCID: PMC5337667.
- Alloimmune Monitoring After Islet Transplantation: A Prospective Multicenter Assessment of 25 Recipients. Delaune V, Toso C, Benhamou PY, Wojtusciszyn A, Kessler L, Slits F, Demuylder-Mischler S, Pernin N, Lablanche S, Orci LA, Oldani G, Morel P, Berney T, Lacotte S. Cell Transplant. 2016 Dec 13;25(12):2259-2268. doi: 10.3727/096368916X692023. Epub 2016 Jun 13. PubMed PMID: 27302287.
- Inhibition of the MAP3 kinase Tpl2 protects rodent and human β-cells from apoptosis and dysfunction induced by cytokines and enhances anti-inflammatory actions of exendin-4. Varin EM, Wojtusciszyn A, Broca C, Muller D, Ravier MA, Ceppo F, Renard E, Tanti JF, Dalle S. Cell Death Dis. 2016 Jan 21;7:e2065. doi: 10.1038/cddis.2015.399. PubMed PMID: 26794660; PubMed Central PMCID: PMC4816180.
- Five-Year Metabolic, Functional, and Safety Results of Patients With Type 1 Diabetes Transplanted With Allogenic Islets Within the Swiss-French GRAGIL Network. Lablanche S, Borot S, Wojtusciszyn A, Bayle F, Tétaz R, Badet L, Thivolet C, Morelon E, Frimat L, Penfornis A, Kessler L, Brault C, Colin C, Tauveron I, Bosco D, Berney T, Benhamou PY; GRAGIL Network. Diabetes Care. 2015 Sep;38(9):1714-22. doi: 10.2337/dc15-0094. Epub 2015 Jun 11. PubMed PMID: 26068866.
- Impact of anti-insulin antibodies on islet transplantation outcome: data from the GRAGIL Network. Lablanche S, Borot S, Thaunat O, Bayle F, Badet L, Morelon E, Thivolet C, Wojtusciszyn A, Frimat L, Kessler L, Penfornis A, Brault C, Colin C, Bosco D, Berney T, Benhamou PY; GRAGIL Network. Transplantation. 2014 Aug 27;98(4):475-82. doi: 10.1097/TP.0000000000000081. PubMed PMID: 24837539.
- Acute nutrient regulation of the mitochondrial glutathione redox state in pancreatic β-cells. Takahashi HK, Santos LR, Roma LP, Duprez J, Broca C, Wojtusciszyn A, Jonas JC. Biochem J. 2014 Jun 15;460(3):411-23. doi: 10.1042/BJ20131361. PubMed PMID: 24678915.
- Proteasome dysfunction mediates high glucose-induced apoptosis in rodent beta cells and human islets. Broca C, Varin E, Armanet M, Tourrel-Cuzin C, Bosco D, Dalle S, Wojtusciszyn A. PLoS One. 2014 Mar 18;9(3):e92066. doi: 10.1371/journal.pone.0092066. eCollection 2014. PubMed PMID: 24642635; PubMed Central PMCID: PMC3958412.
- Comparative impact on islet isolation and transplant outcome of the preservation solutions Institut Georges Lopez-1, University of Wisconsin, and Celsior. Niclauss N, Wojtusciszyn A, Morel P, Demuylder-Mischler S, Brault C, Parnaud G, Ris F, Bosco D, Badet L, Benhamou PY, Berney T. Transplantation. 2012 Apr 15;93(7):703-8. doi: 10.1097/TP.0b013e3182476cc8. PubMed PMID: 22343333.
- Impact of the number of infusions on 2-year results of islet-after-kidney transplantation in the GRAGIL network. Borot S, Niclauss N, Wojtusciszyn A, Brault C, Demuylder-Mischler S, Müller Y, Giovannoni L, Parnaud G, Meier R, Badet L, Bayle F, Frimat L, Kessler L, Morelon E, Penfornis A, Thivolet C, Toso C, Morel P, Bosco D, Colin C, Benhamou PY, Berney T; GRAGIL Network. 2011 Nov 15;92(9):1031-8. doi: 10.1097/TP.0b013e318230c236. PubMed PMID: 21926944.
- Regulated laminin-332 expression in human islets of Langerhans. Armanet M, Wojtusciszyn A, Morel P, Parnaud G, Rousselle P, Sinigaglia C, Berney T, Bosco D. FASEB J. 2009 Dec;23(12):4046-55. doi: 10.1096/fj.08-127142. Epub 2009 Aug 10. PubMed PMID: 19667121.
- Quality of life after islet transplantation: data from the GRAGIL 1 and 2 trials. Benhamou PY, Milliat-Guittard L, Wojtusciszyn A, Kessler L, Toso C, Baertschiger R, Debaty I, Badet L, Penfornis A, Thivolet C, Renard E, Bayle F, Morel P, Morelon E, Colin C, Berney T; GRAGIL group. Diabet Med. 2009 Jun;26(6):617-21. doi: 10.1111/j.1464-5491.2009.02731.x. PubMed PMID: 19538237.
- Immunomodulation by blockade of the TRANCE co-stimulatory pathway in murine allogeneic islet transplantation. Wojtusciszyn A, Andres A, Morel P, Charvier S, Armanet M, Toso C, Choi Y, Bosco D, Berney T. Transpl Int. 2009 Sep;22(9):931-9. doi: 10.1111/j.1432-2277.2009.00892.x. Epub 2009 May 15. PubMed PMID: 19453995; PubMed Central PMCID: PMC2858391.
- Computer-assisted digital image analysis to quantify the mass and purity of isolated human islets before transplantation. Niclauss N, Sgroi A, Morel P, Baertschiger R, Armanet M, Wojtusciszyn A, Parnaud G, Muller Y, Berney T, Bosco D. 2008 Dec 15;86(11):1603-9. doi: 10.1097/TP.0b013e31818f671a. PubMed PMID: 19077896.
- The role of macrophage migration inhibitory factor in mouse islet transplantation. Toso C, Serre-Beinier V, Emamaullee J, Merani S, Armanet M, Wojtusciszyn A, Bosco D, Calandra T, Roger T, Morel P, Shapiro AM, Berney T. Transplantation. 2008 Nov 27;86(10):1361-9. doi: 10.1097/TP.0b013e31818bdbef. PubMed PMID: 19034004.
- Insulin secretion from human beta cells is heterogeneous and dependent on cell-to-cell contacts. Wojtusciszyn A, Armanet M, Morel P, Berney T, Bosco D. Diabetologia. 2008 Oct;51(10):1843-52. doi: 10.1007/s00125-008-1103-z. Epub 2008 Jul 30. PubMed PMID: 18665347.
- The diabetes-linked transcription factor Pax4 is expressed in human pancreatic islets and is activated by mitogens and GLP-1. Brun T, Hu He KH, Lupi R, Boehm B, Wojtusciszyn A, Sauter N, Donath M, Marchetti P, Maedler K, Gauthier BR. Hum Mol Genet. 2008 Feb 15;17(4):478-89. Epub 2007 Nov 7. PubMed PMID: 17989064.
- Expectations and strategies regarding islet transplantation: metabolic data from the GRAGIL 2 trial. Badet L, Benhamou PY, Wojtusciszyn A, Baertschiger R, Milliat-Guittard L, Kessler L, Penfornis A, Thivolet C, Renard E, Bosco D, Morel P, Morelon E, Bayle F, Colin C, Berney T; GRAGIL Group. Transplantation. 2007 Jul 15;84(1):89-96. PubMed PMID: 17627243
- Assessment of 18F-FDG-leukocyte imaging to monitor rejection after pancreatic islet transplantation. Toso C, Zaidi H, Morel P, Armanet M, Wojtusciszyn A, Mai G, Baertschiger R, Buhler L, Berney T. Transplant Proc. 2006 Nov;38(9):3033-4. PubMed PMID: 17112892.
- Detection of insulin mRNA in the peripheral blood after human islet transplantion predicts deterioration of metabolic control. Berney T, Mamin A, James Shapiro AM, Ritz-Laser B, Brulhart MC, Toso C, Demuylder-Mischler S, Armanet M, Baertschiger R, Wojtusciszyn A, Benhamou PY, Bosco D, Morel P, Philippe J. Am J Transplant. 2006 Jul;6(7):1704-11. PubMed PMID: 16827874.
- Sequential kidney/islet transplantation: efficacy and safety assessment of a steroid-free immunosuppression protocol. Toso C, Baertschiger R, Morel P, Bosco D, Armanet M, Wojtusciszyn A, Badet L, Philippe J, Becker CD, Hadaya K, Majno P, Bühler L, Berney T; GRAGIL group. . Am J Transplant. 2006 May;6(5 Pt 1):1049-58. PubMed PMID: 16611343.
- A comparison of cold storage solutions for pancreas preservation prior to islet isolation. Wojtusciszyn A, Bosco D, Morel P, Baertschiger R, Armanet M, Kempf MC, Badet L, Toso C, Berney T. Transplant Proc. 2005 Oct;37(8):3396-7. PubMed PMID: 16298605.
- Logistics and transplant coordination activity in the GRAGIL Swiss-French multicenter network of islet transplantation. MC Kempf, A Andres, P Morel, PY Benhamou, F Bayle, L Kessler, L Badet, C Thivolet, A Penfornis , E Renoult, JM Brun, C Atlan, E Renard, C Collin, L Milliat-Guittard, N Perrin, S Demuylder-Mischler, D Bosco, T Berney.Transplantation. 2005 May 15;79(9):1200-5. PubMed PMID:15880070
- Impact de la variabilité glycémique sur la masse fonctionnelle des cellules bêta pancréatiques. Broca C, Bonnet JB, Gilles J, Granziera S, Armanet M, Wojtusciszyn A. CAD-026. SFD 2019
- Le milieu conditionné de cellules stromales pancréatiques humaines immortalisées : un microenvironnement de soutien bénéfique pour la cellule bêta. Villard O, Armanet M, Wojtusciszyn A. CAD – 023C. SFD 2019

IRMB
Institute for Regenerative Medicine & Biotherapy (IRMB)
Hôpital Saint Eloi
80 rue Augustin Fliche
34295 MONTPELLIER – Cedex 5
FRANCE